Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 15. 06. 2017 10:03 — Editoval Svářeč (15. 06. 2017 10:05)
částice Zn v roztoku
Potřeboval bych poradit s jedním příkladem. Spočítal jsem ho, ale myslím, že asi špatně.
V soustavě Zn(II)/H2O, kde m(Zn) = 0,1 mol/kg, mám vypočítat koncentrace částic přítomných v roztoku (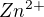 ,
, 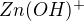 ) a množství vysráženého ZnO v závislosti na pH roztoku. Jiné částice uvažovat nemám. Mám uvažovat ideální chování.
) a množství vysráženého ZnO v závislosti na pH roztoku. Jiné částice uvažovat nemám. Mám uvažovat ideální chování. 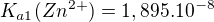 ;
; 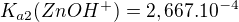
To je doslovné zadání, nic bližšího uvedeno není. K těm konstantám jsem si napsal rovnice
(1)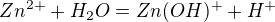
![kopírovat do textarea $K_{a1}=\frac{[Zn(OH)^{+}].[H^{+}]}{[Zn^{2+}]}$](/mathtex/ff/ffbb5ce2f5b84ce7c5333b74e78e91f1.gif)
(2)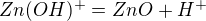
![kopírovat do textarea $K_{a2}=\frac{[ZnO].[H^{+}]}{[Zn(OH)^{+}]}$](/mathtex/93/93a09a2986553e9cbac7a2e36ad731ae.gif)
Následně bilance látkového množství![kopírovat do textarea $m(Zn) = [Zn^{2+}] + [Zn(OH)^{+}] + [ZnO]$](/mathtex/63/63c3d1a440f913ec3a8fafa20239d1ea.gif)
a podmínka elektroneutrality![kopírovat do textarea $2 [Zn^{2+}] + [Zn(OH)^{+}] +[H^{+}] = [OH^{-}]$](/mathtex/84/84537dc970e1f9ef2fb1451bcf2e41d1.gif)
Udělal jsem to jednoduše tak, že z těch rovnic pro K1 a K2 jsem si dosadil do bilance látkového množství tak, abych vyeliminoval vždy 2 ze 3 neznámých a postupně mi vyšly tři rovnice pro závislosti koncetrace Zn2+, ZnOH+ a ZnO na pH. Vůbec jsem nemusel použít podmínku elektroneutrality ani iontový součin vody.
Tady je ten graf, modrá je ZnO, šedá Zn2+ a oranžová Zn(OH)+
a detail
No a jde o to, že když si pro libovolné pH vezmu příslušné koncetrace, dosadím je do podmínky elektroneutrality, vypočítám [OH-], tak pak nevychází iontový součin vody. Nebo naopak, když spočítám [OH-] z iontového součinu vody a dosadím do podmínky elektoneutrality, tak ta nevychází.
Je v mých úvahách něco špatně, nebo např. iontový součin vody nemusí být z nějakého důvodu dodržen? Přijde mi podezřelé, že jsem nemusel použít tu podmínku elektroneutrality.
Děkuji za radu
Offline
#2 18. 06. 2017 14:39 — Editoval pietro (20. 06. 2017 09:42)
Re: částice Zn v roztoku
↑ Svářeč: Ahoj, dal som wolframu spočítať jednu sadu pri počiatočných podmienkach, keď ešte nepridávame protony a potom neskôr som ich pridával.
obrazok zostavenia rovnic
kod pre wolfram...
Solve 111.1=2*x+3*y+z+v, 55.55=x+y+z+v+w,0.1=u+v+w, 1.895E-8=v*y/u,2.667E-4=w*y/v, 1E-14=y*z
výsledky koncentracií
u = 0.0999378 and v = 0.0000177621 and w = 0.0000444296 and x = 55.5498 and y = 0.000106621 and z = 9.37897×10^-11
pH=-log(0.000106621)=3.972157 (už opravené)
w = 0.0000444296
===============================================
Pridajme trochu protonov ...0.1molu
Solve 111.2=2*x+3*y+z+v, 55.55=x+y+z+v+w,0.1=u+v+w, 1.895E-8=v*y/u,2.667E-4=w*y/v, 1E-14=y*z
result
u = 0.1 and v = 1.895×10^-8 and w = 5.05396×10^-11 and x = 55.45 and y = 0.1 and z = 1.×10^-13
to je asi moc vela
pH=1
==================================================
zjemníme...prídavok
np=+0.01mol
Solve 111.11=2*x+3*y+z+v, 55.55=x+y+z+v+w,0.1=u+v+w, 1.895E-8=v*y/u,2.667E-4=w*y/v, 1E-14=y*z
result
u = 0.0999998 and v = 1.89496×10^-7 and w = 5.05375×10^-9 and x = 55.54 and y = 0.0100002 and z = 9.9998×10^-13
pH=1.9991
===================================================
a sledujeme premennú w....množstvo molov ZnO.
ale rád by som to riešil matematicky....sústavou nelineárnych rovníc :-)
Offline
#3 18. 06. 2017 22:07
Re: částice Zn v roztoku
Díky, že sis dal práci, ale asi jsem to nepochopil :) Co myslíš tím, že přidáváme protony? V zadání nic o přidávání protonů není. Kde jsi vzal to číslo 55,5? A to co jsi udělal, to je vlastně řešení toho příkladu nebo jen ověření toho, zda sedí koncentrace H+ a OH- ? Protože řešením toho příkladu mají být křivky pro koncentrace Zn2+, Zn(OH)+ a ZnO, ale tobě tam vyjdou pro tři hodnoty pH nějaké fixní hodnoty. Nějak to nechápu, my jsme se řešení těchto typů příkladů učili úplně jinak, tohle vidím poprvý v životě.
Offline
#4 19. 06. 2017 15:14
Re: částice Zn v roztoku
Nie je to nič zložité, len stroj nám vyriešil 6rovnic o 6 neznámych.Neznáme su x,y...w=počty molov,rovnice sú dva druhy a) lineárne =3rovnice b) nelineárne=3rovnice (pre K1,K2 a ion.sučin vody=1e-14) Lineárne 3rovnice sú vlastne zo zákona zachovania hmoty (počtu atomov H,O,Zn)Do objemu 1 liter vložíme vodu 55.55molov a pridáme zinok 0.1 molu. Nech sa v objeme deje čokolvek (okrem premeny prvkov)celkové počty jednotlivých druhov atómov (H,O,Zn) sú konštantné stále. A to vyjadrujú práve tie tri linearne rovnice. Všetkým 6-tim rovniciam vyhovuje jedno riešenie, na ktorom sa ustália koncentrácie x,y..w. Z toho vyrátame jednak pH=-log(H3O) a tiež ZnO=w. pH vyšlo cca 9.Teraz ked máme stanoviť w=f(pH), tak musíme to pH meniť, a to pridávaním protónov najlepšie zo silnej kyseliny. Fakticky tým zvyšujeme množstvo Hcelkove v roztoku (pôvodne 111.1). Pri nových množstvách Hcelk dáme stroju vyriešiť znovu všetky premenné a hlavne y a w.
Offline
#7 21. 06. 2017 12:12
Re: částice Zn v roztoku
↑ Svářeč: A k tej podmienke elektroneutrality. Myslím, že rozhodujúce sú jednak rovnovážne konštanty a jednak materiálová bilancia. Kedže rovnovážne konštanty máš nábojovo vyvážené, už potom by sme sa o náboje nemali starať. Ióny sú predsa samostatné životaschopné jedince a ich množstvá sú zahrnuté v rovnovážnych konštantách, tak ako ich dodali experimenty.
Offline
