Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 21. 04. 2018 15:16
- Patrik Eiba

- Příspěvky: 57
- Škola: VSB
- Pozice: Student
- Reputace: 0
Fyzika - komprese dusíku
Ahoj, nemohu se dobrat k vyřešení toho příkladu.
Našel jsem podobný ale byl na expanzi...
Offline
#3 21. 04. 2018 23:18 — Editoval MichalAld (21. 04. 2018 23:21)
Re: Fyzika - komprese dusíku
Všechno je bez záruky....
Pro element práce platí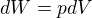
a dále platí stavová rovnice ideálního plynu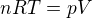
Za předpokladu konstantní teploty tedy platí že:
Po dosazení do vztahu pro prácí máme 
A po integraci dostaneme (integrál z 1/V je ln V)
(je tu ten standardní problém se znaménkem, ale tím já se nemám moc chuť zabývat ... když víme že na stlačení plynu energii potřebujeme. Můžeš si to samozřejmě odvodit nebo najít i se zahrnutím znaménka)
To by nám mělo v principu stačit. Ze stavové rovnice spočítáme počáteční objem (ostatní věci známe, jako tlak, teplotu atd...jen musíme hmotnost plynu v kilogramech přepočítat na moly). Ze vzorce pro práci spočítáme koncový objem, a pak ze stavové rovnice i koncový tlak.
Pak tu máme teplo odevzdané do okolí.
Vnitřní energie ideálního plynu závisí jen na jeho teplotě (na tlaku a objemu nezávisí). Já teď z hlavy nevím, jestli to lze odvodit přímo ze stavové rovnice, nebo je to něco hlubšího (ze statistické mechaniky) ale pro ideální plyn to určitě platí.
Takže všechna práce vykonaná na stlačení plynu se nám změní na teplo, které odevzdáme do okolí - protože při konstantní teplotě (má jít o izotermický děj) se nám vnitřní energie nemění, a na nic jiného než na vnitřní energii nebo odevzdané teplo se práce změnit nemůže. Výsledek tomu i odpovídá, nemusí se nic počítat (jen zase pozor na znaménko...)
A entropie...pro element entropie platí, že
Protože se to vše odehrává při konstantní teplotě, nemusíme nic složitě integrovat, a můžeme rovnou napsat, že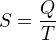
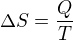
Akorát že to neodpovídá výsledku ... takže je buď špatně výsledek, nebo mám něco špatně já, ale nevím co. Změna entropie s dodanou či odevzdanou prací nesouvisí, jen s dodaným či odevzdaným teplem. Netuším, proč to nevychází.
Koukal jsem i na přímý vzorec pro Entropii ideálního plynu a podle něj by to mělo vycházet taky - protože člen obsahující poměr teplot bude nulový, a druhý člen je stejný jako náš vztah pro výpočet energie, podělený teplotou. Třeba to bude vědět někdo jiný, nebo potvrdí, že je výsledek chybný.
Offline
#4 22. 04. 2018 08:05 — Editoval Patrik Eiba (22. 04. 2018 08:12)
- Patrik Eiba

- Příspěvky: 57
- Škola: VSB
- Pozice: Student
- Reputace: 0
Re: Fyzika - komprese dusíku
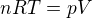 z toho vím že V = nRT/p = tlatk znám, teplotu takym R je konstata 8,314, n = je hmotnost a tu ted mam dat v gramech tedy 3000 ? neni to divné když toto bude v gramech a zbytek bude v základních jednotkách ?
z toho vím že V = nRT/p = tlatk znám, teplotu takym R je konstata 8,314, n = je hmotnost a tu ted mam dat v gramech tedy 3000 ? neni to divné když toto bude v gramech a zbytek bude v základních jednotkách ?
Jinak ty minusi co tam jsou, to jsou zdřejmě pomlčky, takže žadný záporný výsledek nebude.
W = Q to je vyřešeno.
Koncový objem vjádřím z integrované rovnice pro práci a dosadím.
Offline
#5 22. 04. 2018 10:35
Re: Fyzika - komprese dusíku
n není hmotnost, to je látkové množství (v molech), musíš to přepočítat přes molární hmotnost dusíku (tu najdeš v tabulkách).
Ta stavová rovnice plynu se dá napsat také ve fyzikálně jasnějším tvaru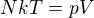
kde N je přímo počet částic a k je Boltzmanova konstantna. Na hmotnosti plynu (hmotnosti jednotlivých atomů) tohle nezávisí, jen na jejich počtu. Musiš se prostě dohrabat k počtu atomů (molekul) plynu. Vyjdadřování počtu atomů v molech (v tom předchozím příspěvku) je jen takové zjednodušení života, a pochází z doby, kdy chemici ještě nevěděli, kolik částic to vlatně je. Dnes už se to ví, ale je někdy lepší psát 1 mol plynu než 6x10^23 částic.
Chemici si oblíbili moly, fyzikové asi raději počítají přímo částice, protože vzorce jsou pak průhlednější.
Podle toho, jestli použiješ skutečný počet částic nebo počet molů částic taky musíš zvolit tu konstantu (k nebo R).
Ty pomlčky jsou opravdu znaménka - ono totiž, pokud bychom zkombinovali více procesů, musíme rozlišovat, jestli práci vykonáváme my (stlačujeme plyn) nebo práci koná plyn (tlačí na píst a my práci získáme). Stejně tak je to s teplem, musíme rozlišovat, jestli teplo dodáváme (ohříváme plyn) nebo odebíráme (ochlazujeme plyn).
Pokud plyn nejdřív ohřejeme a pak ochladíme, musíme dostat původní stav - takže jednou musí být dodané teplo s plusem, podruhé z mínusem (v rovnicích jinak nepoznáme dodané teplo od odebraného).
Znaménka lze odvodit z prvního zákona termodynamiky, který, pokud uvažujeme jen mechanickou práci a dodávání tepla, má tvar: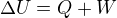
U je vnitřní energie plynu, a znaménka jsou stanovena tak, aby při dodání práce nebo tepla její hodnota vzrostla (i když ono by se nic nestalo, kdybychom to nadefinovali obráceně, energii nelze rozumě měřit). Takže dodávané teplo je s kladným znaménkem, odebírané se záporným. To samé s prací, dodaná je kladná, odebraná záporná.
Offline