Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 22. 05. 2018 19:24
- kockanebopes
- Zelenáč
- Příspěvky: 7
- Reputace: 0
Výpočty z chemické rovnice
Dobrý den,
prosím o pomoc s příkladem:
Kolika procentní roztok KOH vznikne, reaguje-li 9,4 g kovového draslíku s 135 g vody?
Výsledek má být 9,34 %. Bohužel mi počítáním přes molární hmotnosti nevychází.
Předem děkuji.
Offline
#2 22. 05. 2018 19:32
Re: Výpočty z chemické rovnice
Musíš počítat s tím, že část vody se rozloží - bude jí v roztoku méně.
Offline
#3 22. 05. 2018 19:54
- kockanebopes
- Zelenáč
- Příspěvky: 7
- Reputace: 0
Re: Výpočty z chemické rovnice
↑ mák:
Děkuji, já vím. Ale nevím, jak mám vypočítat o kolik.
Zkusila jsem několik postupů:
1. 2M(K) + 2M H2O) ............................ 2M (KOH)
144,4 g .........................................x g
_________________________________________________
144,4 : 114,2 = x : 112,2
x = 141,85 KOH .........100%
9,4 = 6,67 % ...což je špatně
2. jsem zkusila porovnat
2M (H20) ............M (H2)
135g ...................X (H2)
______________________
135 : 36,03 = x : 2,016
x = 7,55 g H2
135 + 9,4 = 144,4 g - 7,55 g = 136,85 g KOH ...... 100%
9,4 g = 6,9 % ....takže taky špatně
Prosím o pomoc, kde pořád dělám chybu. Děkuji.
Offline
#4 22. 05. 2018 20:13
Re: Výpočty z chemické rovnice
Vody zůstane: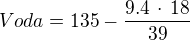
přičemž molekulová váha vody je 18 a draslíku je 39.
Obdobně vypočítáš "vyrobený" louh KOH.
A když máš obě složky, není problém vypočítat hmotnostní koncentraci.
Offline
#5 22. 05. 2018 20:44
- kockanebopes
- Zelenáč
- Příspěvky: 7
- Reputace: 0
Re: Výpočty z chemické rovnice
↑ mák:
Moc děkuji za snahu.
Bohužel jsem v tom čím dál více ztracená. Asi si to nedokážu dost dobře představit. Předpokládala jsem, že voda se rozloží na hydroxid a vodík...tím pádem, že když vypočítám hmotnost vodíku a odečtu od 135 zjistím, kolík jí je v hydroxidu. A když sečtu hmotnost K a hmotnost vody v hydroxidu, vyjde mi hmotnost roztoku... Vím, že je to špatně, ale asi pořád nechápu ten správný princip. Moc děkuji za snahu.
Offline
#6 22. 05. 2018 21:07 — Editoval mák (22. 05. 2018 21:10)
Re: Výpočty z chemické rovnice
Ano, taky to tak můžeš spočítat.
Pokud odečteš vyrobený vodík, zůstane ti směs louhu a vody.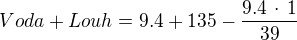
Ale stále potřebuješ spočítat čistý louh, aby si získala koncentraci.
Offline
#7 22. 05. 2018 23:59 — Editoval Kenniicek (23. 05. 2018 00:10)
Re: Výpočty z chemické rovnice
Skusil som ti to vypocitat ciselne, a staci tento, sice nie uplne dokonaly ale jednoduchy postup:
1. spocitat latkove mnozstvo drasliku
2. n(K) sa rovna n(KOH) co plynie z rovnice
3. vypocitat hmotnost KOH
4. plati zakon zachovania hmotnosti, takze hmotnost z 3. staci vydelit (135+9,4)
Ak by sme chceli byt presni, tak od (135+9,4) by sme museli odpocitat hmotnost vzniknuteho vodiku (co je zanedbatelne oproti celkovej hmostnosti, preto to vychadza spravne) za predpokladu, ze vsetok vodik vysumi prec, co tak uplne nie je pravda. :)
Offline