Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 25. 09. 2018 18:00
Faradayová konštanta
Faradayová konštanta F sa dá odvodiť z jeho zákonov ktoré môžeme rozpísať do vzorcov 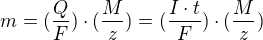 člen
člen 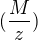 je gram ekvivalent. Pri stanovení konštanty musel odmerať 1A ktorý sa musel rovnať 1C. Z toho už ľahko vypočítal celkový náboj ktorý je potrebný na jeden mol. Bol už vtedy stanovený Ampér alebo zmeral nejakým spôsobom Coulomb. Teoreticky nemusel mať ampér ale musel vedieť koľko coulombov preniesol. Zaujímalo by ma ako to odmeral. Mohol zvážiť váhu striebra, s toho by dostal pomer
je gram ekvivalent. Pri stanovení konštanty musel odmerať 1A ktorý sa musel rovnať 1C. Z toho už ľahko vypočítal celkový náboj ktorý je potrebný na jeden mol. Bol už vtedy stanovený Ampér alebo zmeral nejakým spôsobom Coulomb. Teoreticky nemusel mať ampér ale musel vedieť koľko coulombov preniesol. Zaujímalo by ma ako to odmeral. Mohol zvážiť váhu striebra, s toho by dostal pomer 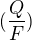 ale musel poznať presný náboj aby mohol vyrátať konštantu
ale musel poznať presný náboj aby mohol vyrátať konštantu
Offline
#2 25. 09. 2018 19:20 — Editoval MichalAld (25. 09. 2018 19:23)
Re: Faradayová konštanta
Historie fyziky se dohledává poměrně těžko, jednak se to dost rychle vyvíjelo, a jednak - co se ukázalo jako chybné bylo dost důkladně "vymazáno z paměti lidstava".
Ale pokud vím, problém nebyl s měřením proudu (ať už byla jednotka definovaná jakkoliv), problém byl s určením velikosti jednoho molu.
A nejsem si tím úplně jistý, ale jestli tomu rozumím správně, tak cesta k určení velikosti molu vedla právě přes stanovení náboje elektronu. A to se muselo udělat úplně jinak...je to nějaký slavný experiment, že se dá na malé kapky vody přenést právě jeden elektron - a z jejich pohybu v el. poli zjistit jeho náboj.
Pak už to jde, když známe náboj elektronu, a změříme náboj potřebný k vyloučení nějakého množství toho uhlíku (který mol definuje), dokážeme už určit, kolik elektronů je ten mol. A na tom, v jakých jednotkách měříme proud, vlastně nezáleží.
Ale tebe asi zajímá něco jiného....
Offline
#3 02. 10. 2018 21:19
Re: Faradayová konštanta
↑ marostul: Ahoj,
množstvá látok vylúčených pri elektrolýzach môžeme spočítať aj bez znalosti Faradayovej konštanty. Postačuje ku tomu len poznatok o elementárnom náboji.
Offline
#5 02. 10. 2018 21:31
Re: Faradayová konštanta
↑ MichalAld: :-) tak ako si poznamenal, história sa ťažko dohľadáva. Predtým v minulosti sme tu mali hádam aj stovku rôznych dĺžkových mier a každá partia si hájila tú svoju.
Offline
#6 02. 10. 2018 22:06
Re: Faradayová konštanta
Zkoušel jsem dohledat, jak se na to v minulosti šlo...
měření elementárního náboje
Překvapilo mě, že regulární metoda je i výpočet z Avogadrovy a Faradayovy konstanty - protože hodnotu Avogadrovy konstanty lze nějak určit přímo - alespoń pro plyny.
Známé je měření nabitých olejových kapek - na které lze přenést i jediný elektron.
S objevem kvantové mechaniky se vynořily další možnosti, jak jej změřit.
Offline
#7 04. 10. 2018 09:11 — Editoval pietro (04. 10. 2018 09:13)
Re: Faradayová konštanta
↑ MichalAld: Michal ahoj,
hodnotu Avogadrovej konštanty udáva "na tvrdo" definícia molu.
Odkaz
==================
aj nejaký prepočet pripájam. :-)
http://forum.matweb.cz/viewtopic.php?id=35959
Offline
#8 04. 10. 2018 23:07 — Editoval MichalAld (04. 10. 2018 23:10)
Re: Faradayová konštanta
pietro napsal(a):
↑ MichalAld: Michal ahoj,
hodnotu Avogadrovej konštanty udáva "na tvrdo" definícia molu.
Odkaz
Myslím, že ještě dnes platí, že je to počet atomů uhlíku C12 ve 12 gramech této látky.
Ale v nejbližší době to bude opravdu pevně dané číslo. To máš pravdu. Ale zatím to tak ještě asi není - a i kdyby už bylo, nic to nemění na faktu, že dost dlouhou dobu se prostě vůbec nevědělo, kolik atomů ten mol vlastně je.
Takže otázka stanovení velikosti Avogadrovy konstanty je fyzikální otázka (musí se to změřit), i když to lze převést na problém stanovení hmotnosti atomu, a nebo stanovení počtu atomů ve známém množství látky.
Není to mimochodem zas tak jednoduché, jak to na první pohled vypadá (a pokud ten názor nesdílíš, tak můžeš uvést nějaký jednoduchý způsob, jak velikost molu určit - samozřejmě bez znalosti toho, kolik váží atomy).
PS: v odkazovaném vlákně zmiňuješ, že by Avogadrova konstanta měla být celé číslo - a to teď, v novém systému jednotek, opravdu bude.
Offline
#9 05. 10. 2018 09:45
Re: Faradayová konštanta
V současné době mi přijde nejjednodušší vzít prostě kousek grafenu vyrobeného z 12C, ten zvážit a pak všechny atomy spočítat na snímku z STM, nebo AFM.
Nebo by se dal z 12C udělat fulleren 540 a nějakou mikromechanikou udělat hromádku s definovaným počtem molekul a tu pak zvážit.
Offline
#10 05. 10. 2018 10:06
Re: Faradayová konštanta
↑ edison:
Na wiki je zmíněna jedna z metod, co se podobá té tvojí - prostě vzít monokrystal velmi čistého křemíku (např) a pomocí rentgenové krystalografie zjistit strukturu krystalové mřížky (vzdálenosti mezi atomy). Což nám umožní spočítat počet atomů v nějakém známém objemu. Nicméně tohle ani AFM není technika 19. století...
Jestli jsem to správně pochopil, tak první úspěšný pokus o stanovení počtu částic v jednom molu PLYNU byl založený na tom, že tlak ideálního plynu nezávisí na hmotnosti těch částic, co plyn tvoří, ale jen na jejich počtu.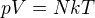
Je to ale pro ideální plyn, a z odkazovaného článku na wiki na první pohled nějak plyne, že se to asi řešilo složitěji, s reálnými plyny (ale já neměl moc chuť to číst, je to dost dlouhé a složité).
Nicméně i v ideálním plynu potřebujeme znát hodnotu Boltzmanovy konstanty, kterou bychom zase museli stanovit nějak jinak (a já nevím jak - statistická mechanika nebyla nikdy má silná stránka). Každopádně to, že pomocí statistických principů bylo možné spočítat atomy v kilogramu plynu je bezesporu dost velký úspěch této teorie (pokud to tak je, já to nevím úplně jistě).
Offline
