Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 06. 10. 2018 12:16
Objem kyslíku za normálních podmínek
Zdravím,
co se chemie týče tak jsem úplný začátečník. Bohužel jsem chemii nikdy moc neřešil (Pouze 2 roky na základní škole a to už bude nějaká doba) a nyní ji mám v prvním semestru na vysoké škole. Máme pouze jednu dvouhodinovou přednášku týdně a žádné cvičení, tudíž mi to nemá kdo pořádně vysvětlit.
Chtěl bych poprosit o vysvětlení tohoto příkladu:
Jaký objem zaujímá za normálních podmínek 62,1 g kyslíku (kyslík tvoří dvouatomové molekuly O2).
Děkuji
Offline
#2 06. 10. 2018 12:25
Re: Objem kyslíku za normálních podmínek
Je to bez záruky, takže by bylo dobré, kdyby to potvrdil ještě někdo další.
Pro ideální plyn platí rovnice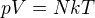
která dává do souvislosti tlak, objem a teplotu plynu s počtem molekul, jež dané množství plynu tvoří. (k je Boltzmanova konstanta)
V chemii se asi častěji používá tvar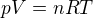
kde je množství plynu uvedeno v počtu molů a né přímo v počtu molekul. Tudíž je tam jiná konstanta (R - nazývá se "univerzální plynová konstanta")
To by mělo podle mě stačit. Je třeba vědět, co jsou to ty "normální podmínky" (je to nějaký tlak a nějaká teplota - to si dohledej), teplota musí být dosazena v kelvinech...
No a pak je třeba určit, kolik molů je těch 62.1 g kyslíku. U toho je třeba vzít v potaz, že tvoří ty dvouatomové molekuly.
Offline
#3 06. 10. 2018 13:52
Re: Objem kyslíku za normálních podmínek
↑ Vacken:↑ MichalAld:
Zdravím.
↑ MichalAld:
Potvrzuji správnost :).
Normální podmínky jsou teplota 0°C (tedy 273,15 K) a tlak 101 325 Pa.
Jen sem ještě přihodím jeden možný postup. Existuje totiž vztah pro tzv. molární objem, který je definovaný jako objem, který zaujme jeden mol ideálního plynu za normálních podmínek.
Přičemž hodnota 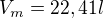
Nicméně tento vztah je vlastně odvozen ze stavové rovnice ideálního plynu. Je úplně jedno, jaká z těchto třech rovnic se použije.
Offline
