Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 05. 12. 2018 11:12
vazebná energie
prosím o pomoc s příkladem. V horních vrstvách atmosféry je molekula O2 rozstepena slunečním zářením na dva atomy kyslíku. Nejdelší vlnová delka fotonu, pro ktery je jev pozorován, má hodnotu 1, 75x10na-7 m. jaka. je vazebna energie molekuly O2? děkuji :)
Offline
#2 05. 12. 2018 19:06
Re: vazebná energie
Aby foton dokázal rozštěpit molekulu kyslíku na dva atomy, musí mít minimálně takovou energii, jaká je energie té vazby (energie potřebná k přerušen vazby, vazebná energie).
A energie fotonu je dle Planckova vztahu 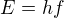
a mezi frekvencí a vlnovou délkou el. mag. vlny je vztah 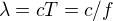
A mmch, pojem "vlnová délka fotonu" není příliš vhodný, vlnovou délku mají vlny (ať už je jejich význam jakýkoliv), foton není vlna, jen se pomocí vln popisuje jeho výskyt.
Offline
#4 06. 12. 2018 22:27 — Editoval MichalAld (06. 12. 2018 22:29)
Re: vazebná energie
Jedna z možností, co mě napadá je, že celá energie fotonu se nemůže použít na ionizaci. Foton má hybnost p=E/c, a tuto hybnost musí mít po srážce i molekula kyslíku (ať už rozštěpená, nebo né).
Můžem to zkusit spočítat (alespoň zjednodušeně):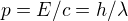
p = 6.63e-34 / 1.75e-7 = 3.79e-27 kgm/s
energie fotonu by byla
E = pc = 1.14e-18 J
Kyslík má atomovou hmotnost zhruba 16, molekula kyslíku tedy zhruba 32. Proton má atomovou hmotnost zhruba 1 a váží mp = 898e-27 kg.
Energie, kterou získá molekula kyslíku po nárazu a zachycení fotonu tedy bude (předpokládejme nerelativistickou situaci, nemyslím si, že by fotony blízkého UV dokázaly urychlovat atomy do relativistických rychlostí):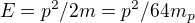
E = (3.79e-27)^2 / (64 * 898e-27) = 2.5e-31 J
To je samozřejmě zanedbatelné vůči energii dopadajícího fotonu, takže tímhle to nebude. Pokud jsem tedy počítal správně.
Nic jiného mě v tuhle chvíli nenapadá. Možná to má ale nějaké jednoduché vysvětlení, jako třeba to, že molekula O2 prostě tyhle frekvence neabsorbuje. Nevím. Taky je samozřejmě možné, že si to zadání někdo jen špatně vymyslel.
Offline
