Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 15. 01. 2008 18:46
Re: Rovnice nedokonaleho horeni
Při hoření uhlíku vznikne energie spalná a světelná.
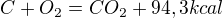 ....... Grammolekula uhlíku /to znamená 12gC / že při úplném spálení
....... Grammolekula uhlíku /to znamená 12gC / že při úplném spálení
je vydáno 94,3kcal.
Spalné teplo na 1g látky je ...7,86kcal.
Jedna krát jedna je " tisíckrát " jedna :-)
Offline
#4 15. 01. 2008 19:37
Re: Rovnice nedokonaleho horeni
No udává se 94,3kcal/mol (tj12gC = 1mol) převod :1cal = 4,18 J...1kcal= 4,18kJ
1. Spalování uhlíku na na oxid uhelnatý je exotermická reakce, teplo se uvolňuje.Teplo,které se uvolní při množství ,která odpovídají stechiometrickým koeficientům v rovnici, je molární teplo reakce.=exotermická
2. U exotermických reakcí má zápornou hodnotu.(Soustava ztrácí energii).Jednotky jsou kJ/mol.
3. Při zápisu reakcí uvedením molárního tepla se uvádí stav reagujících látek.(pevné látky, kap.látky ap).
Tak a dál je to chemie a jestli to násobit dvěmi nevím.
Jedna krát jedna je " tisíckrát " jedna :-)
Offline
#5 15. 01. 2008 21:26
Re: Rovnice nedokonaleho horeni
@ Jelena : Srdečně zdravím,prosím tě, já jsem se pustila do tvého oblíbeného téma, podívej se , co by se k mému příspěvku o hoření dalo ještě přidat.A jestli jsem něco nepopletla.
A taky by mne zajímalo, jestli je to početní řešení správné a celé. Děkuji . Ivana :-)
Jedna krát jedna je " tisíckrát " jedna :-)
Offline
#6 15. 01. 2008 21:40 — Editoval jelena (15. 01. 2008 22:44)
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Rovnice nedokonaleho horeni
To je tak - teplo, ktere potkate v termochemii (spalne nebo slucovaci), se udava v kJ/mol.
Proto reakce se zapise tak, jak ma, je urovnana leva a prava strana, ale pak se to upravi tak, aby "hlavni latka", o ktere mluvime byla vyjadrena jako 1 mol.
2C+ O2= 2CO - puvodni reakce, po uprave (deleno 2:-):
C +1/2 O2 = CO
Pokud se podarilo v tabulkach najit teplo reakce, tak je urcite vztazeno na 1 mol.
Prakticky se to urcuje tak, ze se spali C (grafit) do CO2 a je zmereno spalne teplo, v jinem pokusu se spali CO do CO2 a opet se urci spalne teplo.
Ale teoreticke spalne teplo pri horeni C do CO se musi dopocitavat jako rozdil do dvou predchozich hodnot.
Jelikoz merit spalovani C do CO nema smysl, ve vznikajici smesi jiz vzdy pritomno i CO2 - nemuzeme molekulam CO zakazat, aby se spojovalo s kyslikem, dokud ostatni C nejsou zoxidovany do CO. Jaksi nechapou :-)
Moje tabulky rikaji: teplo vzniku CO2 z C -393,5 kJ/mol, CO2 z CO -283 kJ/mol, rozdil - teoreticke teplo vzniku CO z C je -110,5 kJ/mol. Vsechny hodnoty jsou se znamenkem minus,
Pak v dalsich vypoctech je potreba vychazet z myslenky, ze teplo bylo na mol a bude treba prepocitat kg C (pokud bude zadano) na moly, stejne tak spotrebu kysliku a pod.
Hodne zdaru :-)
Offline