Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 19. 12. 2011 19:22
Chemické reakce -> neutralizace...
Zdravím, sedím nad tím už dlouhý čas, ale ještě jsem nikde nenašel pěkně popsaný postup, jak spočítat nějakou chemickou reakci a následně ji upravit aby se levá strana rovnala pravé. Dokonce ani v učebnici jsem nenašel to co hledám. Chci znát úplné základy a bohužel je to asi tak primitivní, že nevím jak to udělat akorát já a nikde to není napsané.
Např. Al + HCl -> AlCl3 + H2 ; 2Al + 6HCl -> 2AlCl3 + 3H2
- Ale proč je to tak? Jakto že je tam tá trojka AlCl3 ? To bohužel nedokážu pochopit.
Nebo další příklad: H2SO3 + Ba(OH)2 -> BaSO3 + H2O -> tady nevím jak poznám, kolik těch vod bude. Můžete mi to prosím někdo na tomto příkladě stručně vysvětlit? (výpočet rovnice = vznik látky , neutralizace)
Děkuji moc předem za každou odpověď.
Offline
#3 19. 12. 2011 19:49 — Editoval domin.a (19. 12. 2011 19:50)
Re: Chemické reakce -> neutralizace...
↑ domin.a:
a jinak všeobecně zapsaná neutralizace
Neutralizace je reakce kyselin s hydroxidy, při které vzniká voda a sůl:
KYSELINA + HYDROXID → VODA + SŮL
Podstatou neutralizace je reakce vodíkových kationtů s hydroxidovými anionty, při které vzniká voda a uvolňuje se teplo:
H+ + OH- → H2O + TEPLO
Kyselé roztoky lze neutralizovat zásaditými roztoky a naopak.
Příklad neutralizace:
HCl + NaOH → NaCl + H2O
Chlorid sodný (sůl)
Offline
#5 19. 12. 2011 20:01
Re: Chemické reakce -> neutralizace...
↑ ektomorf:
Jedná se o chemickou reakci hliníku Al a kyseliny chlorovodíkové (HCl) k formě Chloridu hlinitého (AlCl3) a vodíku (H2).
Offline
#6 19. 12. 2011 20:15
Re: Chemické reakce -> neutralizace...
↑ domin.a:
A jak poznám, že vznikne zrovna chlorid hlinitý? To je pevně stanoveno?
Zkrátka mám zadáno: Al + HCl ... zbytek musím dodělat sám. Hliník + Chlorovodík, nedokážu poznat, že se jedná zrovna o koncovku -itý. Prosím trochu více popsat proč zrovna tak.
Díky moc.
Offline
#7 19. 12. 2011 22:03 — Editoval o.neill (19. 12. 2011 22:09)
Re: Chemické reakce -> neutralizace...
Je dobré si pamatovat, že některé sloučeniny se vyskutují převážně či výhradně v některých oxidačních číslech. Všechny prvky I.A skupiny mají ve sloučeninách oxidační číslo I, všechny prvky II.A skupiny mají ve sloučeninách oxidační číslo II. Nejsem si jist, zda všechny prvky III.A skupiny (ale pravděpodobně ano) mají ve sloučeninách oxidační číslo III (převážně) a tam patří i hliník. Souvisí to s elektronovou konfigurací ve valenční vrstvě. Prvky I., II., a III. A skupiny mají ve valenční vrstvě pouze jeden, dva respektive tři elektrony a protože se chtějí přiblížit nejbližšímu vzácnému plynu, je pro ně výhodné ztratit všechny tři. Pak je ještě dobré si pamatovat, že zinek má vždycky II, železo II nebo III, měď I nebo II a tak dále a tak dále, v některých tabulkách jsou napsaná běžná oxidační čísla. To všechno nabereš spíš zkušenostmi, asi nemá cenu se to nějak šprtat, prostě až uslyšíš už po milionté, že je něco hlinité a nikdy neuslišíš hlinaté nebo hlinné, tak si to zapamatuješ. Známé jsou ale třeba chytáky, že probíhá reakce
Fe+2HCl ---> FeCl2 + H2,
ale při přímé syntéze vzniká něco jiného
2Fe+3Cl2 ---> 2FeCl3
Offline
#8 20. 12. 2011 19:39
Re: Chemické reakce -> neutralizace...
Díky moc, už se v tom orientuji trochu lépe.
Mohli by jste mi ještě někdo ukázat, jak by to vypadalo třeba s tímto: H2CO3 + Ba(OH)2 ??
Já osobně bych se dostal akorát zde: Ba(CO3)2 + H2O ... dál nevím jak pokračovat - co se týče vyrovnávání stran apod...
Můžete mi popsat postup dokončení této rovnice?
Díky moc.
Offline
#9 20. 12. 2011 20:11
Re: Chemické reakce -> neutralizace...
↑ ektomorf: je to klasická neutralizace kyseliny a hydroxidu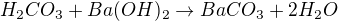
H má téměř vždy oxidační číslo +1 (ty se s vyjímkami nejspíš nesetkáš, takže to ber jako pravidlo)
(OH) má vždy oxidační číslo -1
molekula je vždy neutrální
čili když odebereš 2 vodíky, tak skupina  bude mít oxidační číslo -2. Zbytek je matematika první třídy.
bude mít oxidační číslo -2. Zbytek je matematika první třídy.
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
