Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 10. 06. 2013 18:30
- Matematik12345

- Příspěvky: 129
- Reputace: 0
Kyseliny a zásady
Dobrý den,
chtěl bych poprosit o rychlou pomoc. Potřebuji zjistit, které všechny kyseliny a zásady jsou silné. Našel jsem toto:http://www.aristoteles.cz/chemie/ph/silne-kyseliny.php a toto: http://www.aristoteles.cz/chemie/ph/silne-zasady.php
Ale naše profesorky jich říkala i více. např. říkala, že je silné kyseliny jsou v 1 a ve druhé skupiě a thálium. V aristotelovi je např něco navíc a také zase něco chybí...jsem moc zmatený a potřebuji to pro zítřejší test z hydrolýzy. Byl bych rád, kdybymy to upřesnil někdo :-). Nejlépe i vypsal (pro přehlednost), ale není to podmínkou. budu totiž rád za každou pomoc.
Předem děkuji :-).
Offline
#2 10. 06. 2013 19:20
Re: Kyseliny a zásady
↑ Matematik12345: Ahoj, skús si vyhľadať podobné... ako som nastrelil tu...
http://depts.washington.edu/eooptic/lin … ength.html
http://clas.sa.ucsb.edu/staff/Resource% … 20pKas.pdf
http://www.bluffton.edu/~bergerd/classe … rength.pdf
Offline
#3 31. 07. 2013 11:16
Re: Kyseliny a zásady
Matematik12345 napsal(a):
naše profesorky jich říkala i více. např. říkala, že silné kyseliny jsou v 1 a ve druhé skupiě a thálium.
Pokud tohle opravdu profesorka říkala, tak by měla přestat učit, ale pravděpodobnější je, že jsi nedával pozor a paní profesorka mluvila o silných zásadách.
Offline
#4 02. 08. 2013 10:42
Re: Kyseliny a zásady
S definicí silné zásady bych souhlasil. Silné kyseliny jsou ty, co mají více jak o dva kyslíky víc oproti vodíkům. A pak halogenvodiky od chloru dolů. A pak nějaké ty hexafluoroarseničnany a podobná svinstva.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#5 06. 08. 2013 15:36
Re: Kyseliny a zásady
houbar napsal(a):
a podobná svinstva.
Pár dalších kyselých svinstev jsem seřadil podle hodnoty pKa do přehledné tabulky - http://www.prvky.com/kyseliny.html
Offline
#6 07. 08. 2013 14:29
Re: Kyseliny a zásady
↑ Tackle:
zdar
jednak tam asi máš drobný překlep v kyselině selenové. Druhak se chci zeptat, jak bude vypadat struktura takového zvěrstva, jako je kyselina hexafluoroantimoničná. Antimon tam nemá dost volných "paciček" na všechny fluory a vodík, ne?
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#7 09. 08. 2013 07:49
Re: Kyseliny a zásady
↑ rleg:
Existuje takzvaná koordinační chemie - chemie komplexů. Antimon má volné orbitaly 5d, do kterých může ten šestý fluorid koordinovat.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#8 12. 08. 2013 10:56
Re: Kyseliny a zásady
↑ houbar:
Je to tedy směs  a
a 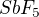 , kde z důvodu, že H má vyšší elektronegativitu než Sb, se atom F raději "přisaje" na Sb a vytvoří tak
, kde z důvodu, že H má vyšší elektronegativitu než Sb, se atom F raději "přisaje" na Sb a vytvoří tak 
Elektronová konfigurace Sb končí  , aby Sb byl pětivazný, změní se jeho konfigurace takto
, aby Sb byl pětivazný, změní se jeho konfigurace takto  . Pak by měl volný orbital 5d, kam by se "přisál" ten 6. atom F. Takhle nějak?
. Pak by měl volný orbital 5d, kam by se "přisál" ten 6. atom F. Takhle nějak?
Radim, tedy jsem.
Dobrá rada je drahá, ta moje je zdarma.
Offline
#9 18. 08. 2013 22:40
Re: Kyseliny a zásady
↑ rleg:
Koordinační chemii nelze takto jednoduše pomocí elektronegativit vysvětlit. Hraje tam roli více faktorů například tvrdost nebo měkkost ligandu. Co se týče elektronové konfigurace atom antimonu či arzénu bude v hybridisaci sp3d2. Všechny orbitaly budou ve stejné slupce. Nikdy nemůžete obsazovat orbital který je ve vyšší slupce než v jaké periodě je atom.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#10 19. 08. 2013 18:21 — Editoval pietro (19. 08. 2013 18:38)
Re: Kyseliny a zásady
Ahojte :-) , myslím, že tá krása (stabilita) priestorovej symetrie hybridizácie sp3d2 nedovolí chudákovi = protónu sa nikde na anión konkrétne naviazať a tak musí plávať ďaleko v roztoku
a páchať takú kyslosť :-(
normálne mi páchla z tohoto videa
Offline
#11 21. 08. 2013 22:26
Re: Kyseliny a zásady
Mimochodem, hexafluoroarseničnany jsou tak kyselé, že dokážou naprotonovat uhlovodík. Z hexanu by potom bylo něco jako C6H15+. Vodík by se tam vázal vazbou asi půltého řádu...
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#13 26. 08. 2013 19:16 — Editoval gorgitko (26. 08. 2013 19:26)
Re: Kyseliny a zásady
↑ houbar: To zas koukám mění můj pohled na chemii :D Ten kladný náboj je v té molekule nějak symetricky rozložen? Protože kde by jinak některý z těch uhlíků vzal místo ještě na půl vazby? Respektive kde by vzal potřebný elektronový pár na vytvoření vazby? (teda přiznávám, že nevím, jakým způsobem funguje vazba půltého řádu...)
Offline
#14 30. 08. 2013 13:28
Re: Kyseliny a zásady
↑ gorgitko:
Omlouvám se, že až teď.
V podstatě tam sdílí tři vazební partneři tři elektrony. Kladný náboj by měl být tedy spíše na atomu uhlíku. Na vzdáleně podobném principu funguje dvojné vazby dusík-kyslík v HNO3...
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#15 13. 10. 2013 21:06
Re: Kyseliny a zásady
Vzpomněl jsem si na to na cvičení z organické chemie a hned po skončení jsem se šel zeptat cvičícího, jestli o tom náhodou něco neví. A věděl, protože se ho na to prý ptali na státnicích před 20 lety :D
Za výzkum karbokationtů byla v roce 1994 udělena Nobelova cena za chemii, a to panu George A. Olahovi. Mimo jiné právě zkoumal protonaci alkanů superkyselinami. Používá se na to velmi silná kyselina HF (flurovodík), jejíž síla je ještě zvýšena přidáním fluoridu antimoničného (SbF5):
SbF5 si přitáhne fluor tak silně, že reakce je silně posunutá doprava a vzniká tak kyselina fluoroantimoničná (HSbF6).
Podle wikipedie je tato kyselina asi  silnější než kyselina sírová (takže bych to odhadl na ten typ kyseliny, do které člověk strčí prst a nevytáhne nic :D).
silnější než kyselina sírová (takže bych to odhadl na ten typ kyseliny, do které člověk strčí prst a nevytáhne nic :D).
Při reakci s methanem pak vzniká karbokation (formálně  ):
):
Doporučuji se podívat do této prezentace, je to tam celkem jednoduše vysvětleno: http://www.nobelprize.org/nobel_prizes/ … index.html
Offline
#16 13. 10. 2013 21:17
Re: Kyseliny a zásady
↑ gorgitko:
HF není silná kyselina. Nemá ani záporné pKa.
Dík za prezentaci.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#18 13. 10. 2013 21:50
Re: Kyseliny a zásady
↑ gorgitko: Máme podobný názor. Já bych se spíš ale přiklonil k tomu, že HF moc silná není, z výše popsaných důvodů.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
