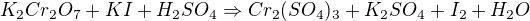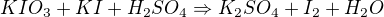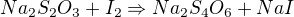Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
Stránky: 1 2
- Hlavní strana
- » Chemie
- » Standardizace odměrného roztoku na primární standart (TOTO TÉMA JE VYŘEŠENÉ)
#26 04. 12. 2016 23:26
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: Standardizace odměrného roztoku na primární standart
Zdravím,
celou diskusi přenechám kolegům, ale toto nelze nechat bez poznámky (viz ↑↑ příspěvek 18: (v originálu žlutě zvýrazněno):
Takže jsem jsem povídal, reakce se mi nezdála správná. Dnes mi ji vrtátily s tím, že standardizace se provádí jinou reakcí, kde musí něco reagovat s jódem! Jedná se o analytickou chemii, nikoliv o anorganickou chemii - vaše rovnice jsou totiž běžně anorganického původu, a proto je v analytice na standardizaci (viz první příspěvek) nelze použít.
↑↑ DTBChemie: Toto tvrzení značí, že zcela ignoruješ principy analytické chemie. Na čem jiném bude metoda postavena, než na chemické reakci vyjadřující vlastnosti sloučenin a jejich vzájemného působení tak, že se výsledek projeví zachytitelnou (pro člověka, nebo pro přístroj) formou a bude zapsán chemickou reakci. Reakce je jen jedna pro každý obor chemie, ať se chemie rozdělí na obory jakkoliv.
Abys dostal požadované 4 rovnice, musíš přeložit do jazyka chemie (což je zápis pomocí chemické reakce nastudované pro tento typ analýz v oboru anorganické chemie) textové sdělení z vašeho materiálu). A to:
a) "standard se nechá reagovat v kyselém prostředí s přebytkem KI",
b) "vyloučený jod se titruje standardizovaným odměrným roztokem thiosíranu".
Tyto 2 reakce jednou zapíšeš pro standard K2Cr2O7, potom pro standard KIO3. Druhá reakce ve dvojici je pořád stejná (I2+Na2S2O3), tak není nutné opakovat zápis (ale zřejmě je požadováno, abys tento zápis zapsal podrobně a odděleně pro každý standard).
↑↑ Bedlasky: dělal a ano "Rovnice jsou tři, ta poslední je druhý krok u obou dvou." :-) jen ke kyselině kolega ↑↑ houbar: povídal výhody použití H2SO4.
Offline
#27 05. 12. 2016 00:16
Re: Standardizace odměrného roztoku na primární standart
↑ jelena:
Zdravím.
Ano, kolega Houbar zmiňoval výhody H2SO4, vím. Jen jsem chtěl říct, že je podstatné to kyselé prostředí. Dokonce se domnívám, že se při té titraci bude H2SO4 používat (ač to tak být samozřejmě nemusí).
Offline
#28 07. 12. 2016 21:15
Re: Standardizace odměrného roztoku na primární standart
Poradíte tedy někdo prosím?
POkud to opravdu udělám podle reackí ve dvou krocích
1) I2 + 2 S2O3(2-) -> 2I- + S4O6(2-)
2) 6I- + BrO3- + 6H+ -> 3 I2 + Br- + 3 H2O
A místo KBrO3 (BrO3-) dosadím své primární stadardy, v prvním příkladě a) K2Cr2O7 b) KIO3 tak jak to tedy bude?
Mám to na ráno, děkuji moc ;)
Offline
#29 07. 12. 2016 21:49
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Když za (BrO3)- dosadíte (IO3)-, co asi tak může vznikat? Na co se bude jodičnan logicky redukovat?
To samé u dichromanu. Jaké oxidační číslo má nejčastěji chrom kromě šestky?
Offline
#30 07. 12. 2016 21:59
Re: Standardizace odměrného roztoku na primární standart
No právě netuším vůbec, takové tvary jsem ještě neviděl nebo jsem nikdy neměl čest takové rovnice tvořit... Poradíte, mi, prosím, jak budou obě reakce?
Co mi poradil internet je tohle: První krok reakce vždy s tím jodem a thiosíranem jsem udělal normálně dle první rovnice v zadání. Pak ale nevím, jak dát druhé reakce primárních stnadardů dát do iontového tvaru.
Poraďte, prosím... 
Offline
#31 07. 12. 2016 22:44 — Editoval Bedlasky (07. 12. 2016 22:47)
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Jak jsem říkal minule, dejte pryč nepodstatné věci. Co je v té reakci podstatné? Co se děje s jodičnanem, co se děje s dichromanem? V jakém to probíhá prostředí? A mimochodem, ta reakce thiosíranu s jodem je až ve druhém kroku. Jak chcete nechat reagovat thiosíran s jodem, když v baňce žádný nemáte?
Offline
#32 07. 12. 2016 23:01
Re: Standardizace odměrného roztoku na primární standart
↑↑ Bedlasky:
Děkuji, moc ;)
Akorát že možná se budete smát, ale já to iontově zkoušel a nemohu to nějak dodělat... Vůbec mi to nejde iontově vytvořit.
Offline
#33 07. 12. 2016 23:26 — Editoval Bedlasky (07. 12. 2016 23:27)
Re: Standardizace odměrného roztoku na primární standart
Bedlasky napsal(a):
Začneme s tou první rovnicí. Chceme ji dát do iontového tvaru. Víme, že dichroman reaguje s jodidem v kyselém prostředí. Tedy, pokud si odmyslíte K+ a (SO4)2- ionty, co Vám zbyde? Obdobně u té druhé.
Offline
#35 07. 12. 2016 23:58
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Říkal jsem pokud si odmyslíte i K+ - ten draslík tam nemá co dělat. Vidíte ho snad na levé straně? Žádné Cr2 tam nebude. Na tu dvojku se momentálně vykašlete. Co to je za kationt? To není chrom.
Offline
#37 08. 12. 2016 00:03 — Editoval Bedlasky (08. 12. 2016 00:04)
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Tak to dejte do té rovnice. Jinak ji máte dobře.
Obdobně postupujete u jodičnanu - K+ a (SO4)2- tam zase nebudou.
Offline
#41 08. 12. 2016 00:16
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Vyčíslené to nemáte. Do reakce vstupuje H+ ne H. Jinak je to dobře.
Offline
#43 08. 12. 2016 00:25
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Ne. Počty jodidů nesedí. Vyčísloval jste to jako redoxní rovnice?
Offline
#44 08. 12. 2016 00:29
Re: Standardizace odměrného roztoku na primární standart
↑ Bedlasky:
Popravdě už chci jít spát... vstávám velmi brzy a nevidím tam již žádnou chybu, Vyčísloval jsem to jen od oka že na levé straně 2 I na pravé I2 to sedí, jinak nevím a už nemůžu čekat jestli to je dobře či nikoliv. Vstávám opravdu brzy a už nemám čas nad tím sedět, bohužel... Jsem myslel, že mi rovnou poradíte třeba a pak bychom to probrali zítra.
Offline
#45 08. 12. 2016 00:34 — Editoval Bedlasky (08. 12. 2016 00:35)
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
Těch jodidů bude víc. Tohle se nedá vyčíslovat od oka. V první rovnici jich bude šest, v druhé pět.
Offline
#47 08. 12. 2016 00:38
Re: Standardizace odměrného roztoku na primární standart
↑ DTBChemie:
U dichromanu šest, u jodičnanu pět.
Offline
#48 08. 12. 2016 00:40
Re: Standardizace odměrného roztoku na primární standart
↑ Bedlasky:
Dobře ale na jaké straně těch 6 a 5 ?
No nic, nechám to tak...
Offline
Stránky: 1 2
- Hlavní strana
- » Chemie
- » Standardizace odměrného roztoku na primární standart (TOTO TÉMA JE VYŘEŠENÉ)