Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#1 20. 03. 2018 23:05
Střední aktivní koeficient
Zdravím.
Chci vypočítat střední aktivní koeficient roztoku NiSO4 o koncentraci 0,1mol/l. Pro výpočet středních aktivních koeficientů jsem našel tento vztah: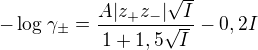
Nejprve jsem začal tím, že jsem si spočítal iontovou sílu:
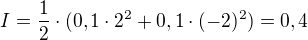
A následně dosadil do výše zmíněného vztahu:
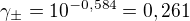
Mělo by to však vyjít 0,180.
Zkoušel jsem i jiné varianty výpočtu - zkoušel jsem počítat aktivní koeficient pro každý ion zvlášť - výpočet je číselně stejný, jako ten výše, až na tu iontovou aktivitu, která je 0,2. Aktivní koeficienty tedy vyjdou pro oba ionty stejné. Potom jsem to dosadil do vztahu:![kopírovat do textarea $\gamma _{\pm }=\sqrt[(\nu _{+}+\nu _{-)}]{\gamma _{+}\gamma _{-}}$](/mathtex/43/43a48bf068cb246d9ef5d52085bb1b7e.gif)
Kde 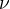 je počet iontů (kladných nebo záporných). Střední aktivní koeficient by se měl tedy v tomto případě rovnat aktivnímu koeficientu jednoho iontu. Tudíž se rovnají i jejich záporné logaritmy. Nicméně, pokud bych porovnal výrazy po dosazení, tak se přeci nerovnají právě kvůli rozdílným iontovým aktivitám:
je počet iontů (kladných nebo záporných). Střední aktivní koeficient by se měl tedy v tomto případě rovnat aktivnímu koeficientu jednoho iontu. Tudíž se rovnají i jejich záporné logaritmy. Nicméně, pokud bych porovnal výrazy po dosazení, tak se přeci nerovnají právě kvůli rozdílným iontovým aktivitám:
V posledním pokusu jsem si spočítal pouze aktivní koeficient síranu a proč výpočet aktivního koeficientu Ni2+ jsem použil tento vztah: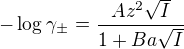
Kde a je iontový poloměr (ten jsem si našel v ve Všeobecné a anorganické chemii od Gaža - 0,069nm). A s tím mi ten výsledek konečně vyšel! Dělal jsem něco v předchozích případech špatně? Nevím proč, ale kdykoliv počítám střední aktivní koeficienty látek, které obsahují dva dvojmocné ionty, nikdy mi to nevychází! Přitom u jakýchkoliv jiných látek, např. NaCl, CoCl2, AlCl3 - to vychází dobře.
Offline
- (téma jako vyřešené označil(a) Bedlasky)
#2 22. 03. 2018 15:55
Re: Střední aktivní koeficient
↑ Bedlasky: Ahoj :-)
pozri prosím aj tu http://www.aqion.de/site/101 koľko rôznych modelov je na to vymyslené.
Offline
