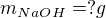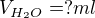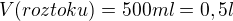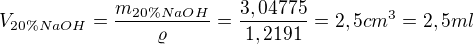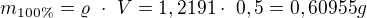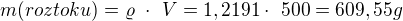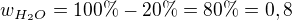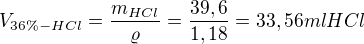Matematické Fórum
Nevíte-li si rady s jakýmkoliv matematickým problémem, toto místo je pro vás jako dělané.
Nástěnka
❗22. 8. 2021 (L) Přecházíme zpět na doménu forum.matweb.cz!
❗04.11.2016 (Jel.) Čtete, prosím, před vložení dotazu, děkuji!
❗23.10.2013 (Jel.) Zkuste před zadáním dotazu použít některý z online-nástrojů, konzultovat použití můžete v sekci CAS.
Nejste přihlášen(a). Přihlásit
#2 16. 10. 2013 10:10
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: příklad - kontrola
Zdravím,
zde je chyba v převodu jednotek (0,5 litru nemůže vážit 0,6 g), překontroluj prosím. Neoznačovala bych indexem _100% protože to plete (v tomto kroku jsi vypočetl celkovou hmotnost 20% roztoku). Dle trojčlenky máme:
celková hmotnost roztoku .................... 100%
hmotnost rozpuštěného NaOH (x) ..............20 %.
Nebo dle hmotnostního zlomku 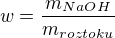 . Další postup je třeba opravit také - je lepší si psát slovní komentář, než bezmyšlenkově používat vzorce. V úvodním tématu je hodně odkazů na takové příklady. Stačí tak? Děkuji.
. Další postup je třeba opravit také - je lepší si psát slovní komentář, než bezmyšlenkově používat vzorce. V úvodním tématu je hodně odkazů na takové příklady. Stačí tak? Děkuji.
Offline
#4 16. 10. 2013 13:58 — Editoval jelena (16. 10. 2013 20:34)
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: příklad - kontrola
↑ Harry:
děkuji, na kalkulačce jsem nekontrolovala, ale už se to zdá být v pořádku, jen bych v druhém řádku napsala do indexu 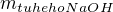 , protože ani ve vzorci pro hmotnostní zlomek nejsou žádná procenta v indexech, ale jen m_složky, m_směsí. Těch 20% v indexu moc smysl nedává, lepší je napsat slovně, pokud potřebuješ "hmotnost tuhého NaOH, co v roztoku činí 20%".
, protože ani ve vzorci pro hmotnostní zlomek nejsou žádná procenta v indexech, ale jen m_složky, m_směsí. Těch 20% v indexu moc smysl nedává, lepší je napsat slovně, pokud potřebuješ "hmotnost tuhého NaOH, co v roztoku činí 20%".
Jeden krok ušetříš, pokud od celkové hmotnosti roztoku 609,55 g rovnou odečteš hmotnost rozpuštěného NaOH (121,91 g), dostaneš hmotnost vody.
A úplně na závěr: není dobré dávat do rovnosti různé jednotky (v posledním řádku, jelikož provádíš přepočet na objem za předpokladu, že hustota vody je 1g/cm^3. Tedy v posledním řádku oddělit: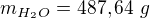 ,
, 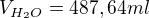
opravena jednotka (cm) u hustoty, děkuji kolegovi houbar.
Offline
#5 16. 10. 2013 15:24 — Editoval jelena (17. 10. 2013 23:13)
Re: příklad - kontrola
↑ jelena:
děkuji, ještě tu mám 1 podobný příklad:
Kolik ml 36%tní kyseliny chlorovodíkové ((ró)=1,18 g/cm^3) je třeba na přípravu 100 ml roztoku o látkové koncentraci c= 0,15 mol/l ((ró)= 1,10 g/cm^3). Mr(HCl)= 36,5
Jelena> Upraveno>
máme roztok 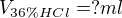
o hustotě 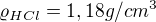
připravujeme roztok 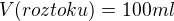
o molární koncentraci 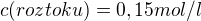
a hustotě 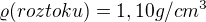
vypočetli jsme hmotnost připravovaného roztoku 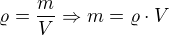

------------------------------------------------------
V tomto roztoku je 0,15 mol/l HCl, tedy ve 100 ml roztoku je n=V*c=0,015 mol, což je m=n*M_r=0,015*36,5 (g HCl).
Toto množství HCl tvoří 36% v roztoku, který máme k dispozici (tedy máme w=0,36, m_složky=0,015*36,5)
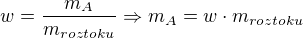
vypočteme hmotnost roztoku, co máme k dispozici 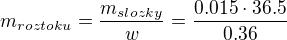
Offline
#6 16. 10. 2013 20:22
Re: příklad - kontrola
Zdravím.
jelena napsal(a):
za předpokladu, že hustota vody je 1g/m^3.
Uteklo vám c, paní kolegyně, správně hustota vody je 1 g/cm^3.
Harry, ten druhý příklad počítáte scestně. Možná by vám mohlo pomoci, kdybyste převedl hmotnostní procenta na molární koncentraci a pak počítal pomocí směšovací rovnice.
Doučím M, Ch v okolí Pardubic
Press any key to continue. Alt + F4?
Offline
#7 16. 10. 2013 20:43
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: příklad - kontrola
↑ houbar:
děkuji, pane kolego, opraveno. Také zdravím.
scestně. Možná by vám mohlo pomoci
přibližně v 2. řádku od konce se podařilo odklonit od správného směru, zvoleného pro řešení. Jiná cesta je dle kolegy ↑ houbar:.
Také by pomohlo, než se dostaví dostatečný nácvik, si u každého výpočtu dopisovat slovní komentář a používat podrobnější značení, než jen "roztok" (ale lepší to psát do komentáře, než do indexu).
Offline
#10 17. 10. 2013 23:33
- jelena
- Jelena
- Místo: Opava
- Příspěvky: 30020
- Škola: MITHT (abs. 1986)
- Pozice: plním požadavky ostatních
- Reputace: 100
Re: příklad - kontrola
↑ Harry:
využila jsem svého Moderátorského práva a napsala jsem komentář přímo do Tvého příspěvku. Zkus si sám ještě jednou projít kroky výpočtu.
Pohodlnější je převést zadanou molární koncentraci  na hmotnostní
na hmotnostní  (nebo naopak) dle vzorce:
(nebo naopak) dle vzorce:
(1) 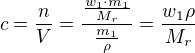
zde  byla hmotnost připravovaného roztoku. Ze vzorce můžeš vyjádřit
byla hmotnost připravovaného roztoku. Ze vzorce můžeš vyjádřit 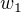 připravovaného roztoku a používat do směšovací rovnice:
připravovaného roztoku a používat do směšovací rovnice: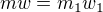 nebo vyjadřovat tak
nebo vyjadřovat tak 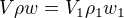 nebo tak
nebo tak 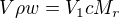 , to jsou jen různá odvození za použití vzorce (1)
, to jsou jen různá odvození za použití vzorce (1)
Než vzorce, bych doporučovala pořádně promyslit, co znamená mít určitý roztok a z něho připravovat roztok jiný, pokud bych si to nepředstavila, tak vzorce neodvodím. Doufám, že v tom nemám nějaký překlep, mohu psát jen v naprostém klidu, ale teď ještě nebyl, pořad se něco požadovalo :-)
Offline